입력 2022-01-05 13:45
- 유혜은 기자
국내외 제약·바이오기업들이 마이크로바이옴(Microbiome)을 활용한 신약 개발에 주목하고 있다. 올해 첫 번째 마이크로바이옴 기반 신약의 탄생을 앞두고 시장 주도권을 잡기 위한 연구·개발(R&D)과 투자가 더욱 활발해질 전망이다.
마이크로바이옴은 미생물(Microbe)과 생태계(Biome)를 합친 말로, 사람의 몸속에 존재하는 수십 조 개의 미생물과 그 유전자를 일컫는다. 일반적으로 몸무게 70㎏ 성인 한 명이 약 38조 개의 마이크로바이옴을 가지고 있는 것으로 알려져 있다.
마이크로바이옴은 건강, 식품, 축산업, 환경 등 다양한 분야에서 활용돼 왔다. 과거에는 식음료 분야에서 주로 쓰였지만, 최근 다양한 질환과 장내 미생물 환경 간의 연관성 등이 밝혀지면서 의약품까지 활용성이 커졌다. 예를 들어 건강한 장내 마이크로바이옴은 소화를 원활하게 하고, 콜레스테롤·혈당 수치 조절과 뇌신경 전달물질 생성에 도움을 준다는 사실이 확인됐다. 이에 따라 소화질환과 비만, 당뇨, 암은 물론 우울증이나 알츠하이머 질환에도 마이크로바이옴이 활용될 수 있다는 연구 결과가 잇따르고 있다.
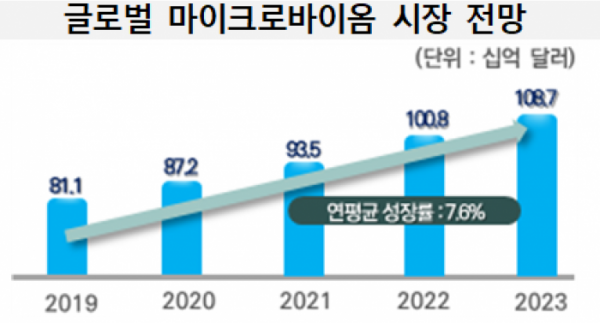
마이크로바이옴 기반 신약 시장은 전 세계적으로 아직 초기 단계이다. 상용화된 의약품은 없지만, 국내외 다양한 회사들이 마이크로바이옴 의약품을 개발하고 있다. 컨설팅업체 프로스트앤드설리번에 따르면 글로벌 마이크로바이옴 시장 규모는 2019년 약 800억 달러(약 96조 원)에서 2023년 약 1100억 달러(약 132조 원)까지 성장할 전망이다.
현재 가장 앞선 것으로 평가받는 기업은 미국 제약사 세레스 테라퓨틱스이다. 세레스는 총 4개의 마이크로바이옴 의약품 파이프라인을 갖고 있다. 대표 파이프라인인 클로스트리듐 디피실 감염증 치료제 'SER-109'는 현재 미국 식품의약국(FDA) 허가 심사 단계다. 연내 결과가 나올 예정으로, 미국 식품의약국(FDA) 허가를 획득하면 최초의 마이크로바이옴 신약 타이틀을 갖는다.
이밖에 이벨로, 4D 파마, 베탄다 바이오사이언스 등이 마이크로바이옴 기반 신약을 개발 중이다. 이벨로는 건선 및 아토피 피부염을, 4D 파마와 베탄다는 고형암을 대상으로 한다. 대부분 임상 1상 혹은 2상 단계다.
글로벌 의약품 시장에서 국내 기업들과 글로벌 선두 제약사들의 연구·개발 격차는 크지만, 마이크로바이옴 시장에서는 격차가 상대적으로 작은 것으로 평가된다. 해외 기업도 대부분 임상 1~2상에 머물러 있다는 점을 감안할때 국내 기업들도 시장 공략에 속도를 내면 해외 기업들과 어깨를 나란히 할 수 있다는 기대가 싹튼다.
업계 관계자는 "마이크로바이옴 의약품 시장은 2026년까지 연평균 93% 성장이 예상되는 유망한 분야"라며 "국내 기업들도 임상 2상이나 1상을 진행 중이기에 적극적인 투자를 바탕으로 격차 축소도 충분히 가능할 것으로 보인다"고 말했다.
우리 정부도 마이크로바이옴에 10년간 1조 원 이상을 지원해 집중 육성하기로 했다. 우선 R&D 혁신을 위해 2023년부터 2032년까지 10년간 1조1506억 원을 투입하는 국가 마이크로바이옴 이니셔티브를 기획·추진, 마이크로바이옴 핵심기술을 확보할 계획이다. 중장기·체계적 지원을 위한 법제도 기반 마련과 국가 마이크로바이옴 빅데이터 구축 계획도 밝혔다.
국내에서 마이크로바이옴 신약을 개발하는 기업은 지놈앤컴퍼니, 고바이오랩, 비피도, 제노포커스 등이 있다. 지놈앤컴퍼니는 면역항암, 뇌질환, 피부질환 등 다양한 마이크로바이옴 파이프라인을 갖고 있다. 현재 고형암 대상 'GEN-001'의 국내 임상 2상과 미국 임상 1/1b상을 진행 중이다.
고바이오랩은 '스마티옴'이란 신약 개발 플랫폼으로 도출한 'KBL697'을 활용한 'KBLP-001'(건선)과 'KBLP-007'(염증성장질환) 등을 보유하고 있다. KBLP-001은 지난달 임상 2상 투약을 개시했으며, KBLP-007은 미국 2a상 임상승인계획(IND)을 받았다.
지난해 7월 CJ제일제당에 인수된 천랩은 5일 CJ바이오사이언스로 공식 출범을 알렸다. 마이크로바이옴 플랫폼 기술을 활용해 2~3년 내 면역항암·자가면역질환 치료용 신약 파이프라인의 미국 임상 진입과 기술수출을 추진할 예정이다.
'지식창고,뉴스 > 마이크로바이옴' 카테고리의 다른 글
| 부광약품, 보장균수 100억 유산균 'BK포스트바이오틱스' 출시 (0) | 2022.01.07 |
|---|---|
| 닻올린 CJ바사 "글로벌 1위 마이크로바이옴 기업 되겠다" (0) | 2022.01.07 |
| 마이크로바이옴 신약개발, 정부에 대기업까지…활성화 조짐 (0) | 2022.01.06 |
| 장내 유익균이 노화 방지 등 건강수명 늘려준다 (0) | 2022.01.03 |
| 해외선 마이크로바이옴 '임상 3상'…뒤늦게 추격나선 K바이오 (0) | 2022.01.03 |



